1. 概要
アメデオ・アボガドロ(1776年 - 1856年)は、イタリアの物理学者、化学者であり、現代化学の基礎を築いた科学者の一人です。彼の最も著名な業績は、同温同圧下においてすべての気体が同体積中に同数の分子を含むという「アボガドロの法則」の提唱です。この法則は、当時の科学界における原子と分子の概念の混乱を解消し、気体が二原子分子から構成されるという画期的な洞察をもたらしました。
彼の功績を称え、物質量(モル)の定義に不可欠な定数である「アボガドロ定数」が彼の名にちなんで名付けられています。この定数は、原子、分子、イオンなどの素粒子の数をモル単位で示すもので、SIの7つの定義定数の一つとされています。アボガドロの理論は発表当初はほとんど注目されませんでしたが、彼の死後、スタニズラオ・カニッツァーロらの努力によってその真価が認められ、原子論・分子論の発展に決定的な影響を与えました。
2. 生涯
アメデオ・アボガドロは、生涯を通じて法学、政治、そして科学の分野で多岐にわたる活動を行いました。その学術的キャリアは、法曹から物理学教授へと転身し、政治的動乱の中で一時的に職を失うも、最終的にはトリノ大学で長きにわたり教鞭を執り続けました。
2.1. 出生と初期の生涯
アメデオ・アボガドロは、本名をロレンツォ・ロマーノ・アメデオ・カルロ・アボガドロ・ディ・クアレーニャ・エ・ディ・チェッレート(Lorenzo Romano Amedeo Carlo Avogadro di Quaregna e di Cerretoイタリア語)といい、1776年8月9日に当時サルデーニャ王国の一部であったトリノで生まれました。彼の家族はクアレーニャとチェッレート・カステッロの伯爵という貴族の家系であり、父親のフィリッポ・アボガドロはサルデーニャ王国の要職を務める法律家でした。母親はアンナ・ヴェルチェッローネ(Anna Vercelloneイタリア語)です。
2.2. 教育
アボガドロは大学で法学と哲学を修め、1796年に20歳(または21歳)で教会法に関する論文を提出し、法学博士の学位を取得しました。卒業後、彼は数年間、父親と同様に法律家、弁護士として法律事務所を開業しました。しかし、1800年代初頭から物理学と数学(当時は「実証哲学」と呼ばれていました)に独学で傾倒し、科学研究を始めました。1803年には、電気工学に関する最初の論文をトリノ科学アカデミーに提出しています。
2.3. 初期のキャリアと学術活動
法曹としての活動を続ける傍ら、科学への情熱を深めたアボガドロは、1806年にはトリノ大学の助教授に就任しました。さらに1809年には、家族が居住し財産を所有していたヴェルチェッリの王立大学で自然哲学の教授として教鞭を執り始めました。このヴェルチェッリでの教授職の期間中、彼は精力的に研究を進め、1811年に彼の最も重要な業績となる論文『物質の基本粒子の相対的質量とこれらの化合比率を決定する一つの方法』(Essai d'une manière de déterminer les masses relatives des molécules élémentaires des corps, et les proportions selon lesquelles elles entrent dans ces combinaisonsフランス語)をフランスの科学雑誌『Journal de Physique, de Chimie et d'Histoire naturelle』に発表しました。この論文には、後に「アボガドロの法則」として知られる彼の仮説が含まれています。当時の北イタリアはフランスの支配下にあったため、論文はイタリア語ではなくフランス語で執筆されました。
2.4. 教授としてのキャリア
1820年、アボガドロはトリノ大学の物理学教授に就任しました。トリノは、ヴィットーリオ・エマヌエーレ1世の下で復興されたサヴォイア家のサルデーニャ王国の首都となっていました。しかし、1822年(または1823年)に政治的な問題に巻き込まれ、教授職を一時的に失うことになります。大学は公式に「この興味深い科学者が重い教育義務から休息を取り、研究に専念できるよう喜んで許可する」と発表しましたが、実際には1821年3月のピエモンテ革命運動への関与が原因でした。彼はごくわずかな年金を受け取り、再び弁護士事務所を開いて科学実験を続けながら弁護士の仕事に戻りました。その後、1833年にトリノ大学に復帰し、さらに20年間教鞭を執り続け、1850年に教授職を退きました。
2.5. 政治的活動と公職
アボガドロは、1821年3月の革命運動(ピエモンテの反乱)に積極的に関与しました。この活動が原因で、彼は1823年に教授職を失うことになります。一部の歴史家は、彼がサルデーニャの革命家たちを支援したと指摘しています。しかし、1848年にカルロ・アルベルト・ディ・サヴォイア王が憲法(アルベルト憲法)を公布する以前から、アボガドロは公職にも就いていました。彼は統計学、気象学、度量衡に関する役職を歴任し、ピエモンテ地方にメートル法を導入する上で重要な役割を果たしました。また、王立公教育高等評議会のメンバーであり、1848年には公教育会議の議員にも選出されています。
2.6. 私生活
アボガドロの私生活についてはほとんど知られていませんが、質素で敬虔な人物であったとされています。彼はフェリチタ・マッツェ(Felicita Mazzéイタリア語)と結婚し、6人の子供をもうけました。
2.7. 死没
アボガドロは晩年までトリノで活動を続け、1856年7月9日に80歳で同地で死去しました。彼の業績が科学界で広く認められるのは、彼の死後4年が経過した1860年のことでした。
3. 科学的業績
アメデオ・アボガドロは、化学および物理学の分野で画期的な発見と貢献をしました。彼の提唱した法則と概念は、現代科学の基礎を築く上で不可欠なものとなっています。
3.1. アボガドロの法則
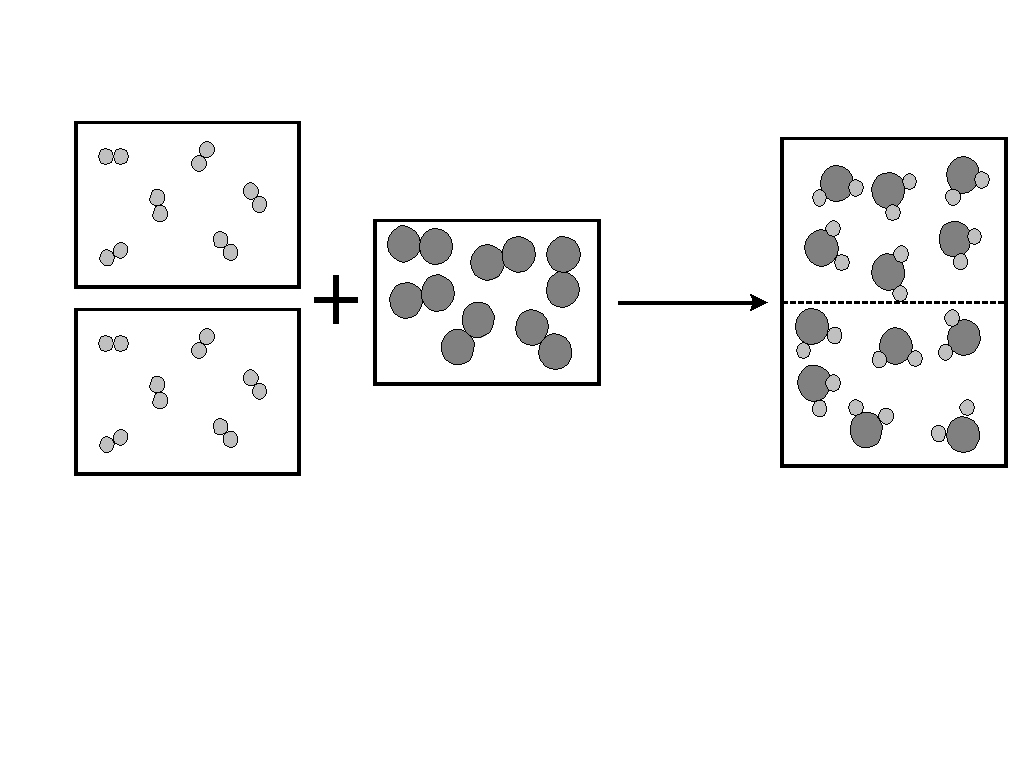
アボガドロの法則は、「同温同圧のもとでは、すべての気体は同じ体積中に同数の分子を含む」というものです。この法則は、1808年にジョゼフ・ルイ・ゲイ=リュサックが発表した気体反応の法則(反応する気体の体積が常に簡単な整数比で示される)を受けて、アボガドロが1811年に提唱しました。
当時の科学界では、ジョン・ドルトンの原子論が広まっていましたが、気体同士の反応を説明する上で矛盾が生じていました。例えば、水素2体積と酸素1体積が反応して水蒸気2体積が生成されるという実験結果は、ドルトンの原子論(H + O → HO)では説明が困難でした。ドルトンは、単一の元素からなる気体は単一の原子から構成されると信じていたため、体積比と粒子数比が一致しない場合が生じたのです。
アボガドロは、この問題を解決するために二つの画期的な仮説を提示しました。第一に、同単位の気体は同じ体積を占めること、そして第二に、気体は単一の原子ではなく、同種の原子が二つ結合した「二原子分子」からなるというものです。この分子仮説と組み合わせることで、上記の反応は2H2 + O2 → 2H2Oと表され、実験結果の2対1対2という体積比を直接的に説明できるようになりました。アボガドロの最初の仮説自体は当時も存在しましたが、二番目の分子仮説と結びつけることでその真価を発揮しました。この法則は、今日でも化学教育の初年度で必ず扱われる重要な基本法則です。
アボガドロの着想は唯一無二でさえない。例えば、電流の単位であるアンペアとして名が残るフランスの物理学者アンドレ=マリ・アンペールはアボガドロとは独立に1813年、同様の法則を考案している(やはり再評価前には注目されていない)。しかし、気体反応の法則を初めて定式化したのは、アボガドロである。
(*)0℃、1.013×105Pa(パスカル)で、1mol 6.0221×1023個の気体分子を集めると、その種類によらず22.414 リットルとなる。
3.2. 原子と分子の区別
アボガドロの最も重要な貢献の一つは、当時の科学界で混同されていた原子と分子の概念を明確に区別したことです。彼は、気体は分子から構成され、これらの分子はさらに原子から構成されると主張しました。ドルトンはこのような可能性を考慮していませんでした。アボガドロ自身は「原子」という言葉を直接使わず、「基本分子」という言葉で現在の原子に相当する概念を表現しました。彼はまた、質量と重量の定義についてもより詳細な注意を払いました。
アボガドロは、この概念に基づいて、1811年に水、硝酸、亜硝酸、アンモニア、一酸化炭素、塩化水素の正しい分子式を提示しました。さらに1814年には、二酸化炭素、二硫化炭素、二酸化硫黄、硫化水素の分子式も提示しています。彼はまた、自身の法則を金属にも適用し、17種類の金属の原子量を計算する試みも行いました。
3.3. アボガドロ定数
アボガドロの分子論への貢献を称え、物質1モルに含まれる素粒子の数(原子、分子、イオン、その他の粒子)は「アボガドロ定数」NAと名付けられています。この定数の値は正確に6.02214076 × 1023であり、SIを定義する7つの定数の一つです。アボガドロ定数は、化学反応の計算に用いられ、与えられた反応で生成される物質の量を高い精度で決定することを可能にします。
アボガドロ定数の値は、ヨハン・ヨーゼフ・ロシュミットが最初に計算しました。ドイツ語圏の国々では、この定数が「ロシュミット数」と呼ばれることもありましたが、現在では「ロシュミット定数」は別の意味を持っています。
3.4. 主要な著作
アボガドロは、彼の科学的発見を多くの論文や著作を通じて発表しました。
- 1811年: 『物質の基本粒子の相対的質量とこれらの化合比率を決定する一つの方法』(Essai d'une manière de déterminer les masses relatives des molécules élémentaires des corps, et et les proportions selon lesquelles elles entrent dans ces combinaisonsフランス語)
- 1815年: 『単純な物体の分子の相対質量、またはそれらのガスの推定密度、およびそれらの化合物の構成に関する覚書、1811年7月の『Journal de Physique』に掲載された同主題の試論の続編として』(Mémoire sur les masses relatives des molécules des corps simples, ou densités présumées de leur gaz, et sur la constitution de quelques-uns de leur composés, pour servir de suite à l'Essai sur le même sujet, publié dans le Journal de Physique, juillet 1811フランス語)
- 1821年: 『結合における決定された比率の理論に関する新たな考察、および物体の分子の質量の決定について』(Nouvelles considérations sur la théorie des proportions déterminées dans les combinaisons, et sur la détermination des masses des molécules des corpsフランス語)
- 1821年直後: 『有機化合物を決定された比率の通常の法則に還元する方法に関する覚書』(Mémoire sur la manière de ramener les composès organiques aux lois ordinaires des proportions déterminéesフランス語)
- 1837年から1841年にかけて、彼の主要な著作である『可秤物質の物理学、すなわち物体の物質的構成に関する論文』(Fisica dei corpi ponderabili, ossia Trattato della costituzione materiale de' corpiイタリア語)を全4巻で出版しました。
3.5. その他の研究分野
アボガドロは、アボガドロの法則以外にも多岐にわたる科学的研究を行いました。彼は電気、液体の蒸留、比熱、毛細管現象、原子の体積に関する多くの論文を執筆しています。特に、電気に関する研究は彼の初期の学術活動の始まりであり、1803年にはこの分野で最初の論文を提出しています。
4. 理論への反応と再評価
アボガドロの理論は、発表当初は科学界からほとんど注目されず、その重要性が理解されるまでに長い時間を要しました。しかし、彼の死後、後続の科学者たちの努力によって再評価され、現代化学の基礎として確立されました。
4.1. 初期の受容と無視
アボガドロの仮説は、発表当初の科学界ではほとんど注目されず、すぐには受け入れられませんでした。彼の論文は難解であったこと、また彼自身が国外ではほとんど無名であったこと、さらには他の化学者との交流が消極的であったことなどが、その理由として挙げられています。彼自身が自身の研究を引用する習慣があったことも、当時の学会での認知度を高める妨げになった可能性があります。
アボガドロの死後、電流の単位であるアンペアとして名を残すフランスの物理学者アンドレ=マリ・アンペールも、アボガドロとは独立に1813年に同様の法則を考案しましたが、彼の理論も同様に無視されました。
4.2. 再評価と承認
アボガドロの業績が再評価されるのは、彼の死後4年が経過した1860年のことでした。イタリアの化学者で政治家でもあったスタニズラオ・カニッツァーロが、1858年に発表した論文『ジェノヴァ大学に於ける化学理論講義概要』と、1860年にドイツのカールスルーエで開催された国際化学者会議での発表を通じて、アボガドロの法則の重要性を力説しました。
カニッツァーロは、アボガドロの法則が一部の無機物質で矛盾するように見えた原因が、特定の温度での分子解離によるものであることを説明し、この法則が分子量だけでなく原子量も決定できることを示しました。また、シャルル・フレデリック・ジェラールやオーギュスト・ローランといった科学者たちが有機化学の研究を通じて、アボガドロの法則がなぜ気体中の分子の同量が同体積を持つのかを説明できることを示しました。
さらに、ルドルフ・クラウジウスが1857年に提唱した気体分子運動論は、アボガドロの法則のさらなる証拠を提供しました。ヤコブス・ヘンリクス・ファン・ト・ホッフは、アボガドロの理論が希薄溶液においても成立することを示しました。
1911年には、アボガドロの1811年の古典的な論文発表から100周年を記念する会議がトリノで開催されました。この会議にはイタリア王ヴィットーリオ・エマヌエーレ3世も出席し、アボガドロの化学への多大な貢献が正式に認められました。
5. 影響と遺産
アボガドロの科学的発見は、その後の化学および物理学の発展に計り知れない影響を与え、現代科学の基礎を築きました。彼の業績は、今日に至るまで様々な形で記念され、その遺産は科学の世界に深く刻まれています。
5.1. 科学的発展への貢献
アボガドロは、「原子分子説」の創始者として高く評価されています。彼の法則と、原子と分子を明確に区別する概念は、化学および物理学の基礎を確立し、その後の科学的進歩に不可欠な基盤を提供しました。特に、理想気体の計算における基礎となり、粒子数の計算が重要な学問分野において、気体を利用できるという画期的なアイデアをもたらしました。彼の洞察がなければ、現代化学の発展は大きく遅れていたでしょう。
5.2. 記念と追悼
アボガドロの功績を称えるため、様々な記念が設けられています。
- アボガドロ定数: 物質1モルに含まれる素粒子の数を示す定数であり、彼の名にちなんで名付けられました。
- アボガドライト: 彼の名にちなんで名付けられた鉱物です。
- アボガドロ: 月のクレーターの一つも彼の名が冠されています。
- 1911年には、彼の1811年の論文発表から100周年を記念する国際会議がトリノで開催され、彼の業績が改めて世界的に認められました。
6. 関連項目
- アボガドロの法則
- アボガドロ定数
- モル
- 気体反応の法則
- 原子論
- 理想気体